納米醫(yī)學(xué)(Nanomedicine���,NMs)致力于通過(guò)改造納米材料開(kāi)發(fā)新的治療工具�,將藥物或診斷試劑靶向輸送到病變部位�����,從而打破診斷和治療醫(yī)學(xué)發(fā)展的困境���。近幾十年來(lái)�,無(wú)數(shù)的研究成果革新了治療的方式��,豐富了高精度診斷方法����。未來(lái),納米藥物甚至可以通過(guò)調(diào)整其表面化學(xué)性質(zhì)��、形狀和大小以及識(shí)別群體來(lái)實(shí)現(xiàn)個(gè)性化的治療和診斷��,從而達(dá)到理想的治療效果�����。納米藥物的藥物評(píng)價(jià)對(duì)于納米藥物進(jìn)一步產(chǎn)業(yè)化和臨床應(yīng)用具有重要意義�����。隨著納米技術(shù)的發(fā)展�����,精細(xì)納米復(fù)合材料的優(yōu)化和操作以及表面相互作用的研究越來(lái)越受到重視,利用納米復(fù)合材料可以進(jìn)一步提高體內(nèi)治療效果�,降低副作用。
因此��,了解結(jié)構(gòu)-功能關(guān)系的內(nèi)在聯(lián)系仍然是納米醫(yī)學(xué)發(fā)展的第一要?jiǎng)?wù)����,特別是對(duì)納米藥物體內(nèi)行為的無(wú)創(chuàng)可視化。為了應(yīng)對(duì)這些挑戰(zhàn)�,化學(xué)家和生物學(xué)家在開(kāi)發(fā)原位監(jiān)測(cè)體內(nèi)納米藥物代謝行為的成像技術(shù)方面做出了巨大努力。目前的方法主要是將化學(xué)標(biāo)記嵌入納米藥物中���,包括熒光探針�、光聲試劑�、同位素標(biāo)記等�。這些探針的一個(gè)共同的局限性是它們的空間分辨率相對(duì)較低,尤其是對(duì)于深部組織�。因此,對(duì)體內(nèi)納米藥物在深部組織中的代謝和分布進(jìn)行監(jiān)測(cè)仍然面臨挑戰(zhàn)���。近年來(lái)��,近紅外二區(qū)(NIR-II�,1000-1700nm)成像技術(shù)以其低背景噪聲、高空間分辨率�、高靈敏度等優(yōu)點(diǎn)成為腫瘤和腦深部成像的一種新的工具,并在臨床前藥物開(kāi)發(fā)中發(fā)揮著重要作用��。近幾年在近紅外-Ⅱ技術(shù)方面取得的成就已經(jīng)證明可以在高分辨率下實(shí)現(xiàn)20毫米的組織穿透���。然而���,具有高性能的NIR-II發(fā)光團(tuán)仍然很少見(jiàn),許多發(fā)光團(tuán)在NIR-II處的信號(hào)很弱����。基于供體-受體-供體(D-A-D)的主鏈結(jié)構(gòu)�,近紅外-Ⅱ試劑已被廣泛構(gòu)建。用于構(gòu)建NIR-II發(fā)射分子的受體核通常僅限于苯并雙噻唑(BBT)單元����。
因此,尋找可供選擇的NIR-II核心單元以擴(kuò)展為具有明顯NIR-II信號(hào)的NIR-II材料庫(kù)是一個(gè)根本性的挑戰(zhàn)�����。在本研究中�����,研究者試圖探索噻二唑苯并三唑(BTZ)作為一種可替代的近紅外-Ⅱ型熒光團(tuán)(DTTB),它在808nm處具有13.4%的高熒光量子產(chǎn)率和4.9×104L mol-1cm-1的大吸收系數(shù)�����。此外�����,獲得的NIR-II熒光團(tuán)DTTB被結(jié)合到聚乙二醇膠束中�,以非侵入性地方式顯示納米藥物在體內(nèi)的代謝行為(圖1)。利用全身成像技術(shù)����,研究了納米膠束的PEG長(zhǎng)度對(duì)其在血液中循環(huán)時(shí)間的影響。通過(guò)NIR-II熒光和光聲雙模成像可以清楚地顯示腫瘤的靶向性���。此外��,優(yōu)化后的納米藥物經(jīng)近紅外輻照后,實(shí)現(xiàn)了高效的腫瘤清除�。這項(xiàng)工作提供了一種替代性的高熒光近紅外-Ⅱ熒光團(tuán),可用于體內(nèi)納米藥物的實(shí)時(shí)藥物評(píng)價(jià)���。
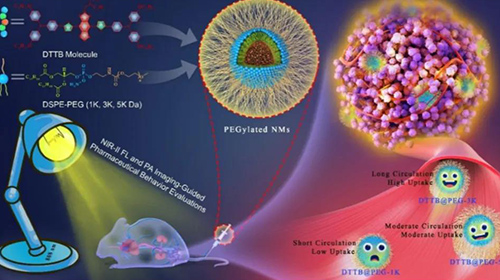
圖1. 利用近紅外-Ⅱ熒光和光聲雙模型成像實(shí)時(shí)評(píng)價(jià)聚乙二醇化納米藥物的藥物行為示意圖
該研究合成一種可替代的D-A-D共軛低聚物(DTTB)��,其N(xiāo)IR-II發(fā)射峰在~1000nm處��,熒光量子產(chǎn)率高達(dá)13.4%��,吸收系數(shù)高達(dá)4.9×104?L mol-1?cm-1�。通過(guò)將DTTB分子結(jié)合在DSPE-PEG上得到三種DTTB@PEG,制備出具有不同鏈長(zhǎng)PEG修飾的NMs�����,并表現(xiàn)出了固有的熒光和光聲成像能力�。采用NIR-II熒光和光聲成像技術(shù),以實(shí)時(shí)�、無(wú)創(chuàng)的方式,對(duì)NMs的聚乙二醇化相關(guān)藥物行為進(jìn)行了綜合評(píng)價(jià)�。
實(shí)驗(yàn)方法
體內(nèi)光聲成像
小鼠麻醉,氧氣流量為2 L/min����,混合3%異氟醚,并在37℃的加溫動(dòng)物床上保持麻醉狀態(tài)���。圖像是通過(guò)Vevo LAZR系統(tǒng)(FUJIFILM VisualSonics, Toronto, Canada)獲得的����。帶有4T1腫瘤(皮下)的BALB/c裸鼠靜脈注射聚乙二醇化NM(DTTB@PEG-1K, DTTB@PEG-3K,和DTTB@PEG-5K���;100μL����,1.0 mg/mL)�����,當(dāng)腫瘤體積約為100 mm3時(shí)�。在680、730�、790和910nm的激光照射下,在注射后不同時(shí)間采集光聲圖像�����。
實(shí)驗(yàn)結(jié)果
納米藥物(NMs)的結(jié)構(gòu)特性(表面�����、形狀����、成分和尺寸)對(duì)其在體內(nèi)的藥物特性有很大的影響。尤其是用聚乙二醇(PEG)修飾NMs的表面��,即PEG化后���,可通過(guò)避免NMs的聚集和吞噬來(lái)延長(zhǎng)NMs的系統(tǒng)循環(huán)時(shí)間��,從而提高NMs輸送到目標(biāo)組織的概率���。盡管聚乙二醇化對(duì)NMs系統(tǒng)藥代動(dòng)力學(xué)的影響已經(jīng)被研究了幾十年,但對(duì)這一問(wèn)題的深入研究卻很少以實(shí)時(shí)可見(jiàn)的方式進(jìn)行�����。與傳統(tǒng)的藥物評(píng)價(jià)方法相比����,生物醫(yī)學(xué)成像技術(shù)(MRI、PET�、photo imaging等)具有無(wú)創(chuàng)性的特點(diǎn),無(wú)需犧牲大量動(dòng)物即可實(shí)現(xiàn)體內(nèi)藥效學(xué)行為的實(shí)時(shí)監(jiān)測(cè)和定量��。將活體成像技術(shù)應(yīng)用于藥物評(píng)價(jià)����,可以大大提高制藥行業(yè)從實(shí)驗(yàn)室概念到商業(yè)產(chǎn)品的效率�����。因此��,在DTTB體外良好的近紅外熒光特性的基礎(chǔ)上��,研究者通過(guò)NIR-II熒光和光聲雙模成像來(lái)評(píng)價(jià)NMs與各種PEG配體在體內(nèi)的藥物分布���。制備了一個(gè)小的納米藥物庫(kù),這些納米藥物與各種PEG配體結(jié)合�����,包括DTTB@PEG-1K, DTTB@PEG-3K��,和DTTB@PEG-5K���。以聚乙二醇化NMs為研究對(duì)象��,研究了PEG鏈長(zhǎng)度對(duì)4T1荷瘤小鼠體內(nèi)給藥效率和藥代動(dòng)力學(xué)的影響���。NIR-II熒光成像和光聲成像如圖2所示�。注射后6-24小時(shí)�,腫瘤區(qū)域的近紅外-Ⅱ熒光強(qiáng)度和光聲強(qiáng)度均顯著增加����,由于增強(qiáng)的通透性和EPR效應(yīng),聚乙二醇化NMs在腫瘤區(qū)域逐漸積聚�����。聚乙二醇化NMs在腫瘤區(qū)域的富集也通過(guò)光聲和熒光信號(hào)強(qiáng)度在體內(nèi)進(jìn)行半定量(圖2B和D)�����。值得注意的是DTTB@PEG-3K在腫瘤部位的信號(hào)增強(qiáng)最為明顯�。于注射后36h采集小鼠主要臟器和腫瘤組織,用NIR-II熒光成像法進(jìn)行組織分布定量����。雖然在肝臟和脾臟中觀察到最強(qiáng)的熒光,但與其他器官相比���,腫瘤呈現(xiàn)出非常明顯的熒光信號(hào)��。圖2E中的量化報(bào)告顯示DTTB@PEG-3K(10.16±2.95%ID/g)相比于DTTB@PEG-1K(3.44±1.21% D/g)和DTTB@PEG-5K(5.41±1.55% ID/g)攝取效率最高�。這意味著NMs的腫瘤部位積聚與PEG鏈長(zhǎng)度有關(guān)。對(duì)NMs在血管中的循環(huán)行為進(jìn)行詳細(xì)的無(wú)創(chuàng)體內(nèi)研究�����,結(jié)果表明了DTTB@PEG-3K具有更長(zhǎng)的循環(huán)壽命��。此外���,藥代動(dòng)力學(xué)研究證實(shí)了DTTB@PEG-3K(1.49小時(shí))相比于TB@PEG-1K(0.54小時(shí))和DTTB@PEG-5K(0.95小時(shí))在體內(nèi)停留的時(shí)間更長(zhǎng)����。納米顆粒表面能呈現(xiàn)出不同的PEG分子構(gòu)象狀態(tài)��,這與PEG鏈長(zhǎng)和納米粒子表面的PEG密度密切相關(guān)��。納米粒子表面PEG層的結(jié)構(gòu)構(gòu)象對(duì)納米粒子在血清中的膠體穩(wěn)定性和蛋白質(zhì)吸附有顯著影響����,從而對(duì)納米粒子在血液中的循環(huán)時(shí)間有根本性影響。因此��,研究者TTB@PEG-3K的循環(huán)時(shí)間較長(zhǎng)是由于PEG分子表面的構(gòu)象����,DTTB@PEG-3K能有效地抑制補(bǔ)體化合物在納米粒子上的吸附��,導(dǎo)致單核吞噬細(xì)胞系統(tǒng)(MPS)對(duì)納米粒子的攝取減少���,有助于延長(zhǎng)血液循環(huán)時(shí)間。
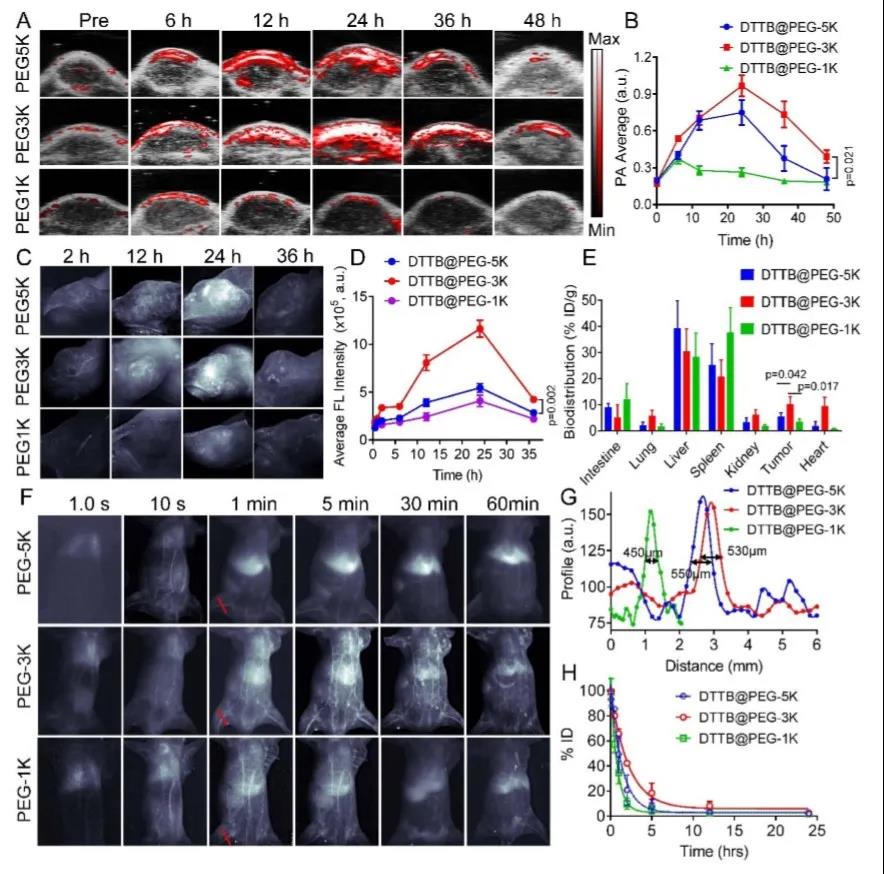
圖2. 4T1荷瘤小鼠靜脈注射后不同時(shí)間獲得的具有代表性的體內(nèi)光聲圖像(A)和DTTB@PEG-1K, DTTB@PEG-3K��,和DTTB@PEG-5K在NIR-II熒光圖像(C)
4T1腫瘤區(qū)不同時(shí)間光聲(B)和NIR-II熒光(D)信號(hào)的半定量分析��。E����、 DTTB@PEG-1K, DTTB@PEG-3K����,和DTTB@PEG-5K注射后36小時(shí)的體內(nèi)分布。F�����、 實(shí)時(shí)記錄裸鼠靜脈注射后60分鐘內(nèi)的活體血管成像DTTB@PEG-1K, DTTB@PEG-3K��,和DTTB@PEG-5K�����。G、 基于橫截面剖面的Vesselwhm寬度分析(F中的紅線)��。H����、 DTTB@PEG-1K,和DTTB@PEG-5K靜脈注射后的藥物動(dòng)力學(xué)分析�����。擬合曲線為R2值分別為0.9756���、0.9961和0.9882的單相衰減函數(shù)���。循環(huán)半衰期(t1/2)分別為0.95、1.49和0.54小時(shí)(數(shù)據(jù)以平均值±標(biāo)準(zhǔn)差表示�,n=3。統(tǒng)計(jì)學(xué)分析采用雙尾不配對(duì)t檢驗(yàn))�����。
結(jié)論
綜上所述�����,研究者利用NIR-II熒光納米平臺(tái)對(duì)聚乙二醇化納米藥物進(jìn)行實(shí)時(shí)藥劑學(xué)評(píng)價(jià)的方法。所設(shè)計(jì)的NIR-II發(fā)光體在808nm處具有較大的吸收系數(shù)�����,在NIR-II窗口具有較高的熒光量子產(chǎn)率����。用NIR-II型發(fā)光體結(jié)合聚乙二醇化形成納米藥物并監(jiān)測(cè)其再體內(nèi)的代謝行為。體內(nèi)NIR-II熒光和光聲成像結(jié)果表明����,適當(dāng)?shù)木垡叶蓟兄谘娱L(zhǎng)在血液中停留的時(shí)間�����、提高腫瘤靶向性及良好的生物安全性����,從而實(shí)現(xiàn)長(zhǎng)循環(huán)NIR-II納米藥物的高效光熱治療。本研究提出了一個(gè)在體內(nèi)對(duì)納米藥物進(jìn)行實(shí)時(shí)藥物評(píng)價(jià)的方法�����,并展示了NIR-II納米平臺(tái)在納米藥物開(kāi)發(fā)中的潛力。